一、痛风石的形成过程
痛风石是由细胞裂解后的释放的细胞膜于细胞器碎片、蛋白、DNA等组分会包裹尿酸盐晶体形成
痛风石主要存在于两个部位:① 两个关节间的滑囊腔;② 关节周围的肌肉内
关节间的滑囊腔中的痛风石会造成严重的关节损伤,除了疼痛、水肿外,一般没有其他显著症状
关节肌肉内的痛风石,会在皮肤表面形成“鼓包”
只要痛风发作过,关节间的滑囊腔中就存在痛风石,但是关节周围内的肌肉内未必有
只要皮肤表面形成了“鼓包”,则关节周围的肌肉内必有痛风石,滑囊腔中也必有痛风石
痛风患者的痛风石最先形成于滑囊腔中,沉积的痛风石会损伤关节和关节周围的肌肉,随后尿酸盐晶体会进入肌肉内,皮肤表面形成“鼓包”状的痛风石
不同患者出现肌肉内痛风石的时间是不同的,有些人时间段、有些人时间长
若高血尿酸、痛风未有效治疗,5 年后 12% 患者出现痛风石,20 年后痛风石的比例为 70%
痛风石的形成过程总共分为 3 步[1,2]:
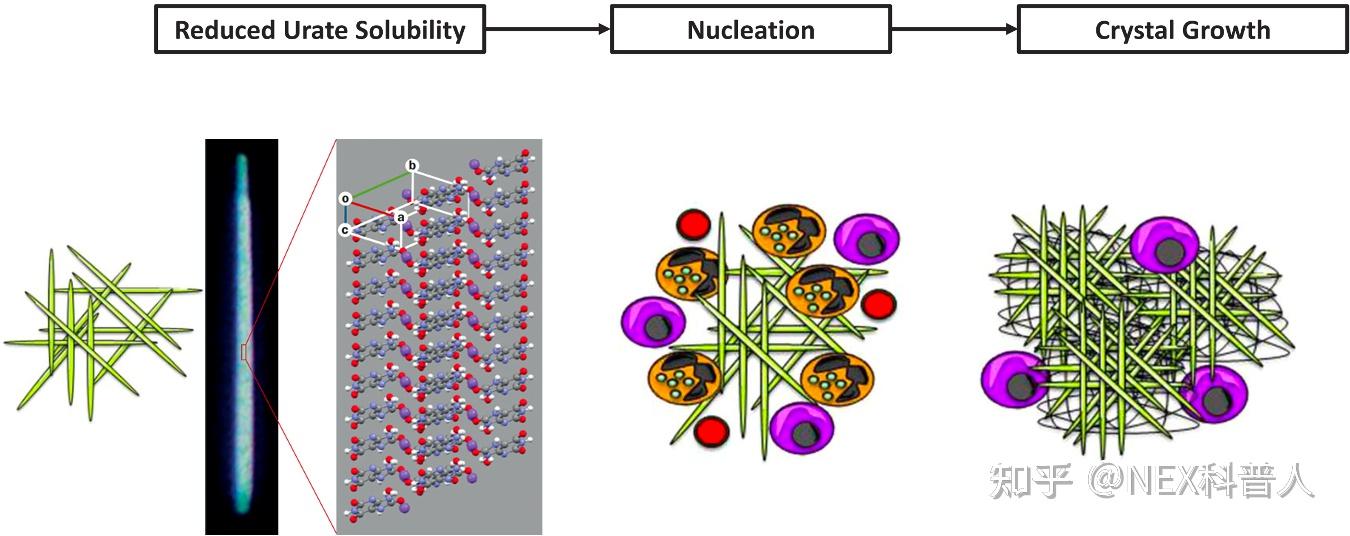
第一步:析出尿酸盐晶体:是痛风石的起点,也是最关键的因素
血尿酸升高或者影响尿酸盐溶解的因子变化后,关节内会析出尿酸盐晶体
痛风是由尿酸钠(MSU)晶体沉积引起的最常见的炎性关节病,最初人们认为尿酸盐晶体沉积只发生在关节周围软组织,但最近的研究表明,尿酸盐晶体沉积也存在于四肢关节外部位[3~6],脊椎[7]、心血管内[3,8,9]、泌尿系统内[3,10,11]、心脏等其他组织器官内[3,12]。
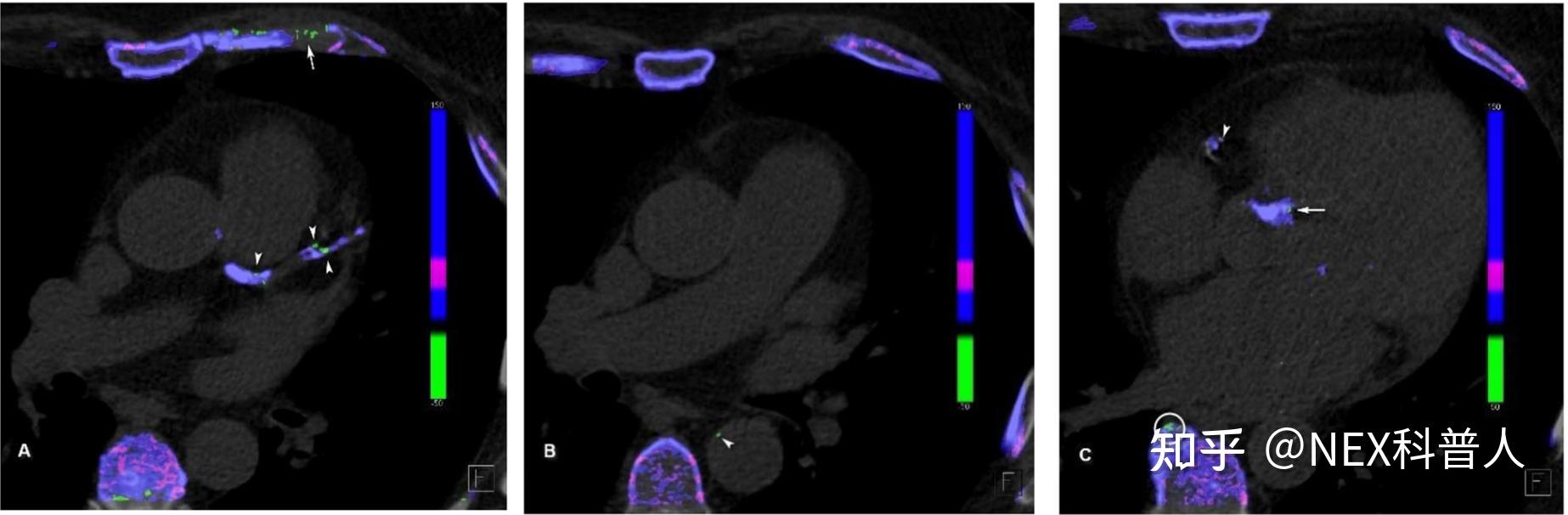
新血管内尿酸盐晶体沉积
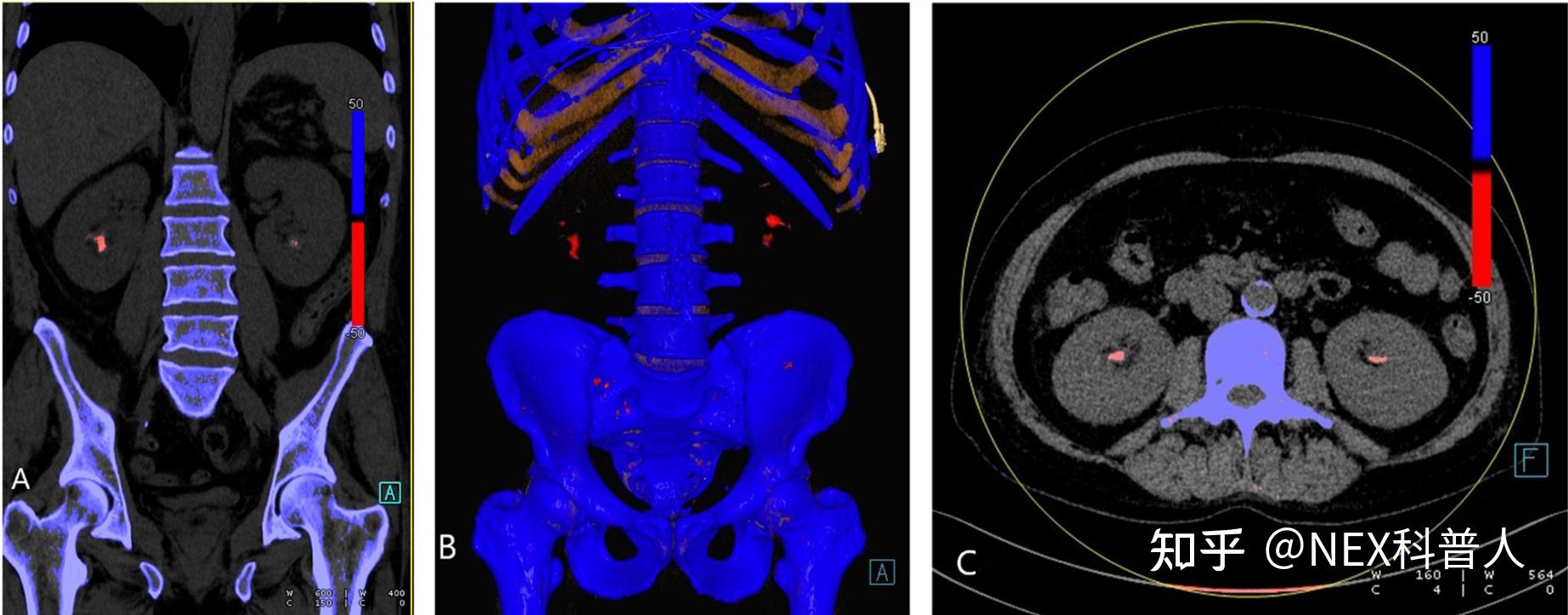
肾内尿酸盐晶体/尿酸类肾结石
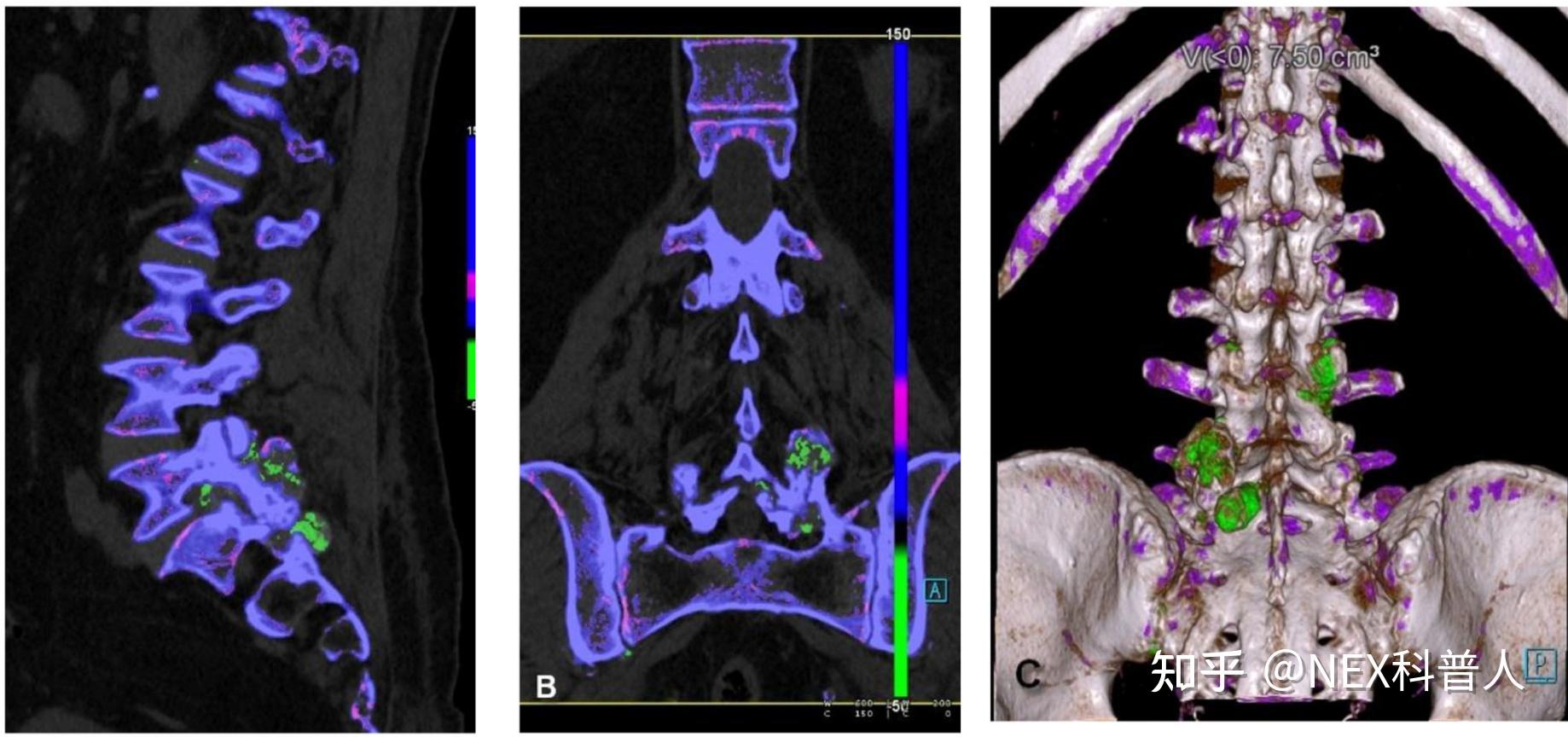
脊椎内尿酸盐晶体
影响尿酸盐晶体形成因素主要有[13]:
- 血尿酸水平、形成尿酸盐晶体的组织器官内的尿酸浓度
- 血液与形成尿酸盐晶体的组织器官之间实现物质交换的难易程度
- 温度:如果关节受凉导致滑囊液温度降低,会使滑囊液中的尿酸溶解度降低,析出尿酸盐晶体,导致痛风发作
- pH 值:尿酸盐在 pH≤5.5(尿酸)或≥10(重尿酸盐) 溶解度高,pH 5.5~8(单质子尿酸盐)时溶解度最低(在此范围内,pH 越低,尿酸盐溶解度越低),若过度劳累、运动过度、关节受伤或其他关节疾病导致关节内滑囊液 pH 发生变化,也会导致东风发作
- 阳离子浓度:尿酸与K+、Mg2+、Cu2+等离子形成的尿酸盐溶解度高于与Ca2+、Na+形成的尿酸盐,尤其是 K+ 可以竞争性替换尿酸钠盐中的Na+。Na+、NH4+、Ca2+等离子促进尿酸盐结晶形成,K+、Mg2+、Cu2+等离子抑制尿酸盐形成。因此,若关节疾病、药物、生活习惯等导致Na+、NH4+、Ca2+等离子浓度升高,而K+、Mg2+、Cu2+等离子浓度降低,也会导致痛风发作
- 软骨蛋白多糖、硫酸软骨素、人血清白蛋白、低浓度透明质酸盐均可以提高尿酸盐溶解度,若疾病、药物、生活习惯等导致其降低,也诱使痛风发作
- 尿酸盐晶体可以粘附抗体蛋白,中85%为IgM、14%为IgG,均促进尿酸盐晶体成核、增长。若疾病、药物、生活习惯等导致关节内抗体蛋白含量增加,也诱使痛风发作
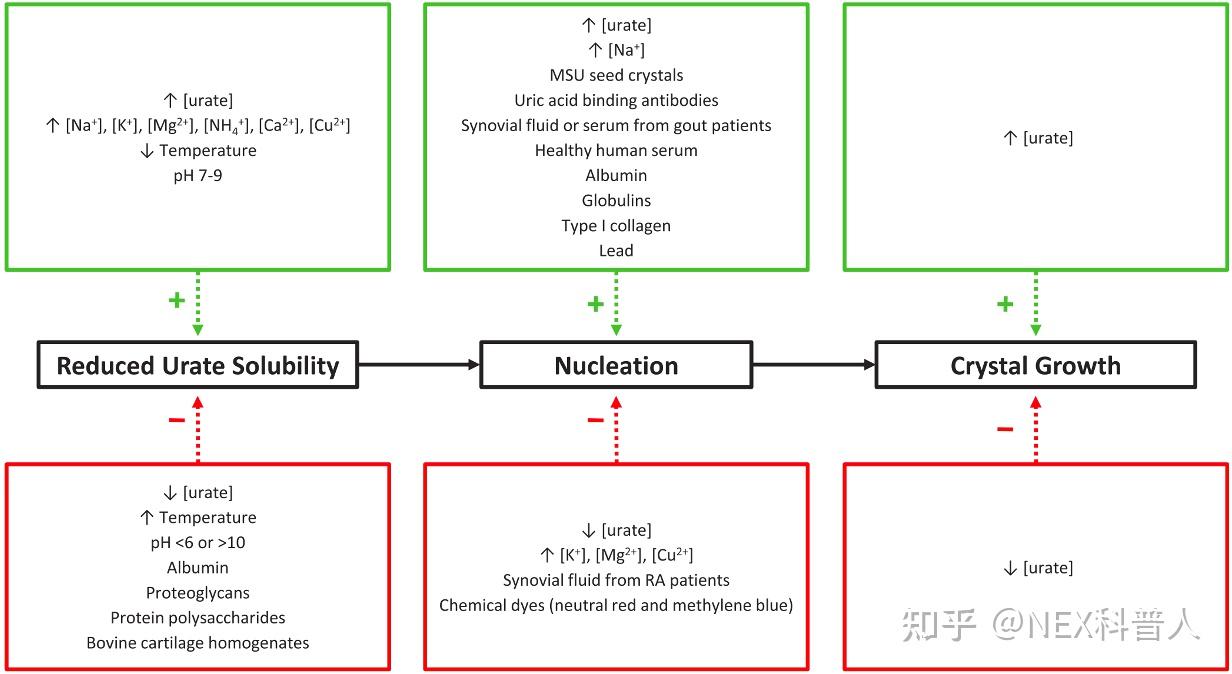
影响尿酸盐晶体形成和溶解的因素
第二步:尿酸盐晶体成核,形成痛风石的最小单位 NETs 结构
形成尿酸盐晶体后,关节处的炎性因子 IL-1β 表达、成熟、分泌量急剧升高
促炎因子招募大量的中性粒细胞,使关节炎症级联放大,促使关节内的中性粒细胞出现细胞焦亡、裂解,细胞残余组分(主要是细胞膜组分、细胞器组分、蛋白质、DNA等)会包裹析出的尿酸盐晶体,形成 NETs 结构
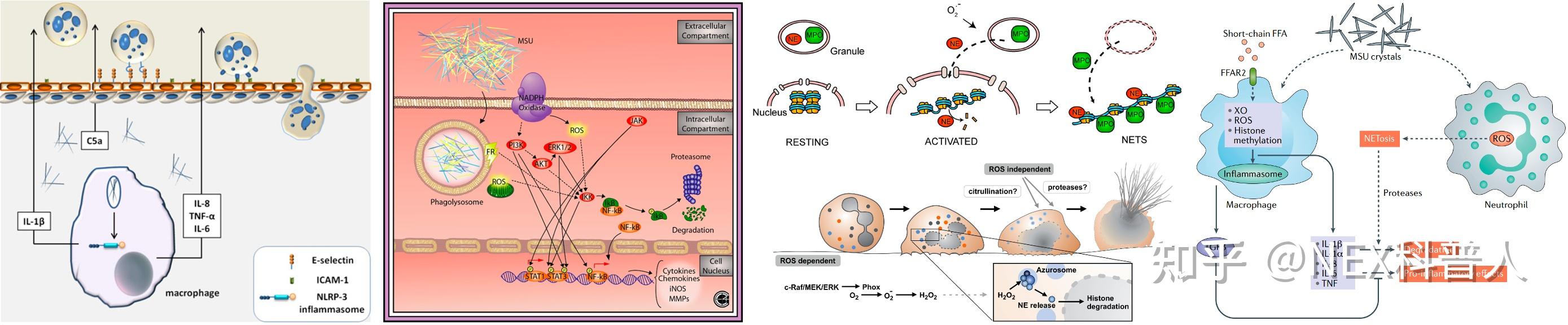
NETs 结构的形成过程
影响尿酸盐晶体成核速度的关键点是尿酸盐晶体的促炎活性
尿酸盐晶体表面亲水能力强,可以吸附调控蛋白和其他血液因子,引发不同的细胞反应
IgG、C5a、C1q、CD14 等吸附于尿酸盐晶体表面后,可以被巨噬细胞、肥大细胞等TLRs/IL-1R等受体结合,激活 NF-kB 通路,诱导 IL-1β 等细胞因子的表达,激活炎症反应
ApoB、ApoE、LDL 等吸附于尿酸盐晶体表面后,抑制被招募的中性粒细胞分泌炎性因子的能力,缓解炎症
另外,尿酸可以与K+、Mg2+、Cu2+、Ca2+、Na+、NH4+等离子形成尿酸盐,尿酸钾的溶解度最高、促炎活性最弱,尿酸钠的溶解度最低、促炎活性最强[14]。
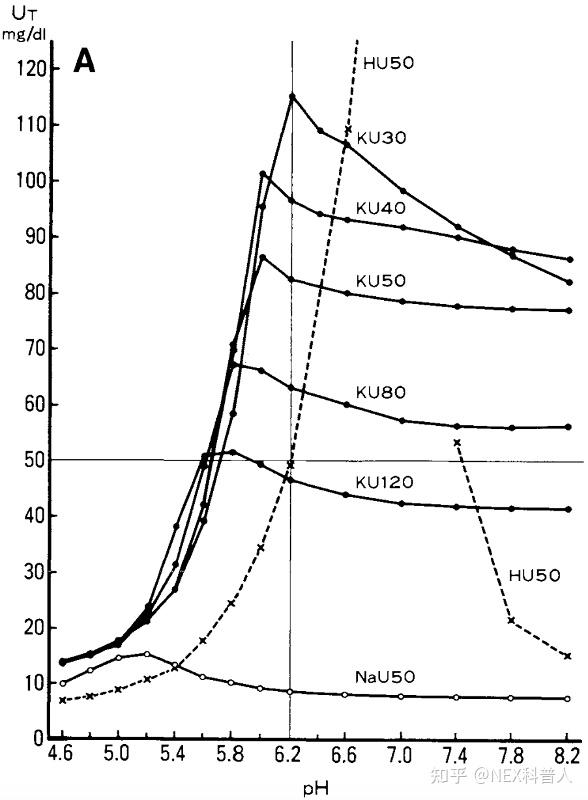
Schorn C 等研究人员发现尿酸钾晶体诱发氧化应激、促炎能力都显著弱于尿酸钠晶体[15]。

尿酸钠晶体与尿酸钾晶体促炎能力的差异
第三步:痛风石增大
NETs结构相互聚集沉淀形成 aggNETs,aggNETs 结构较大、溶解度很低,会相互聚集沉淀致使痛风石增大
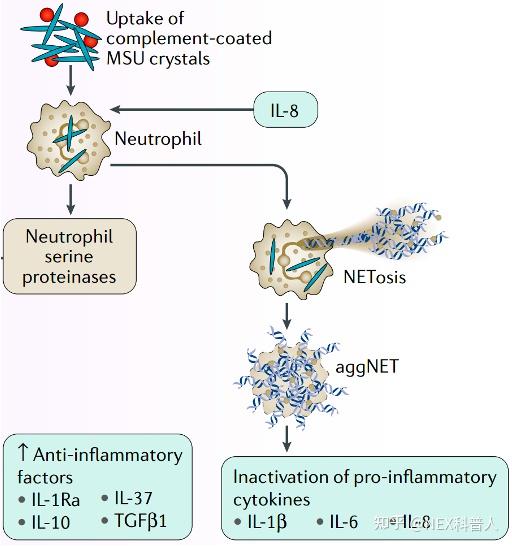
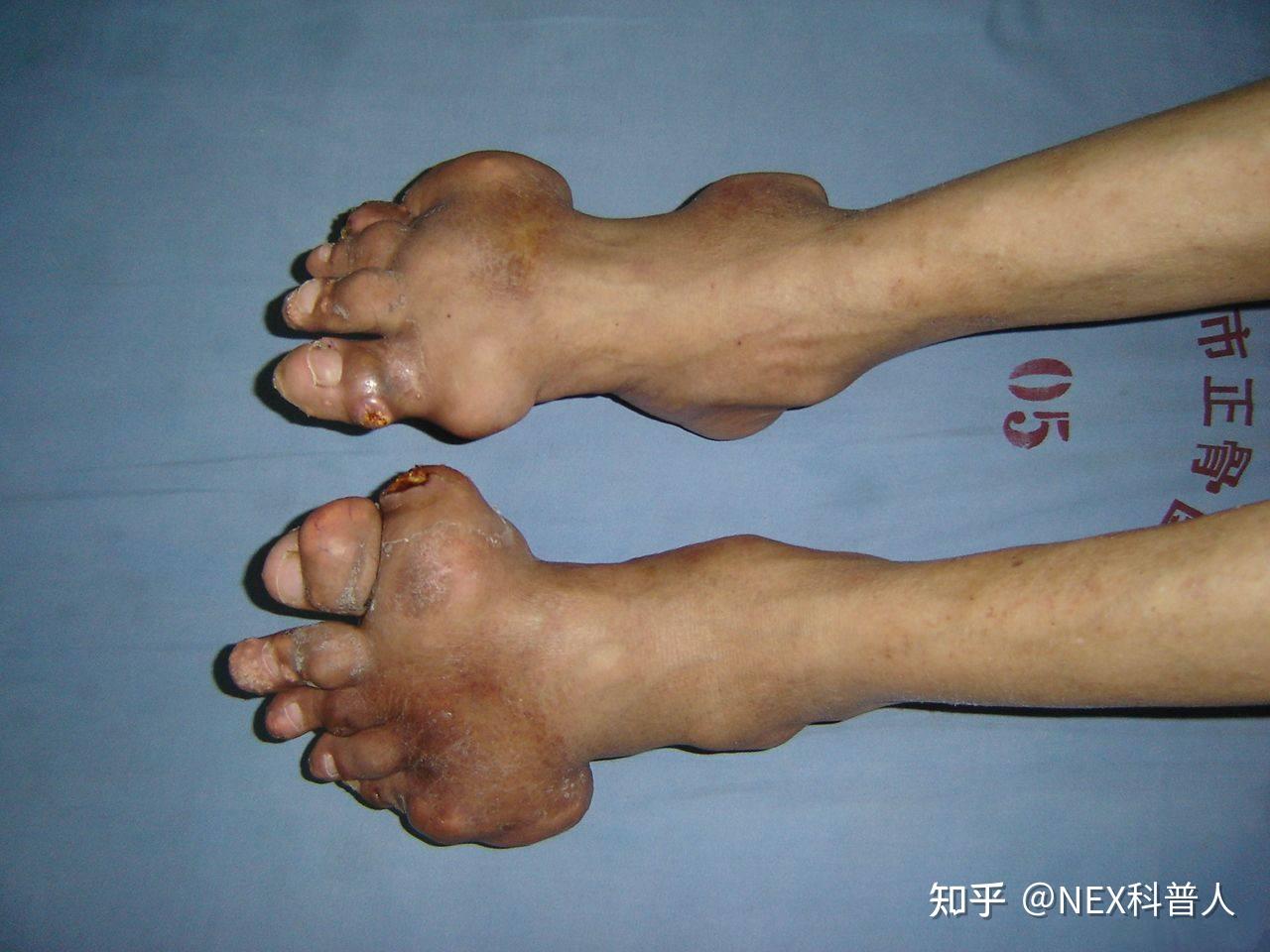
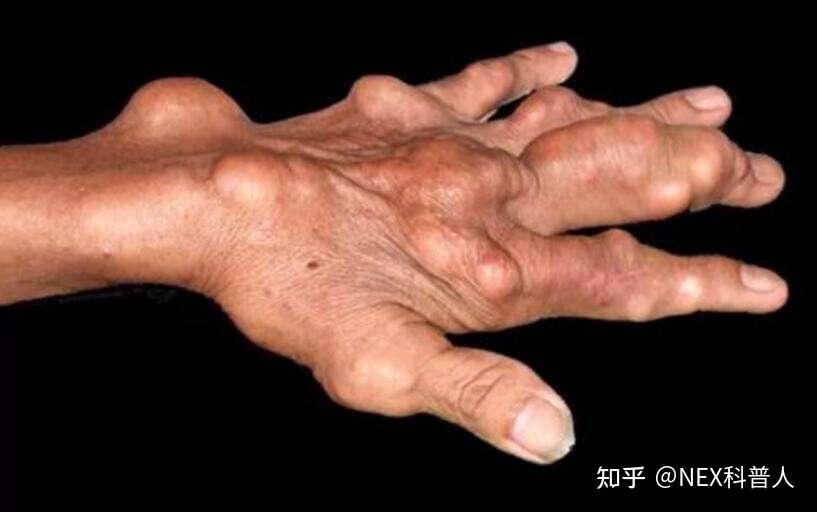
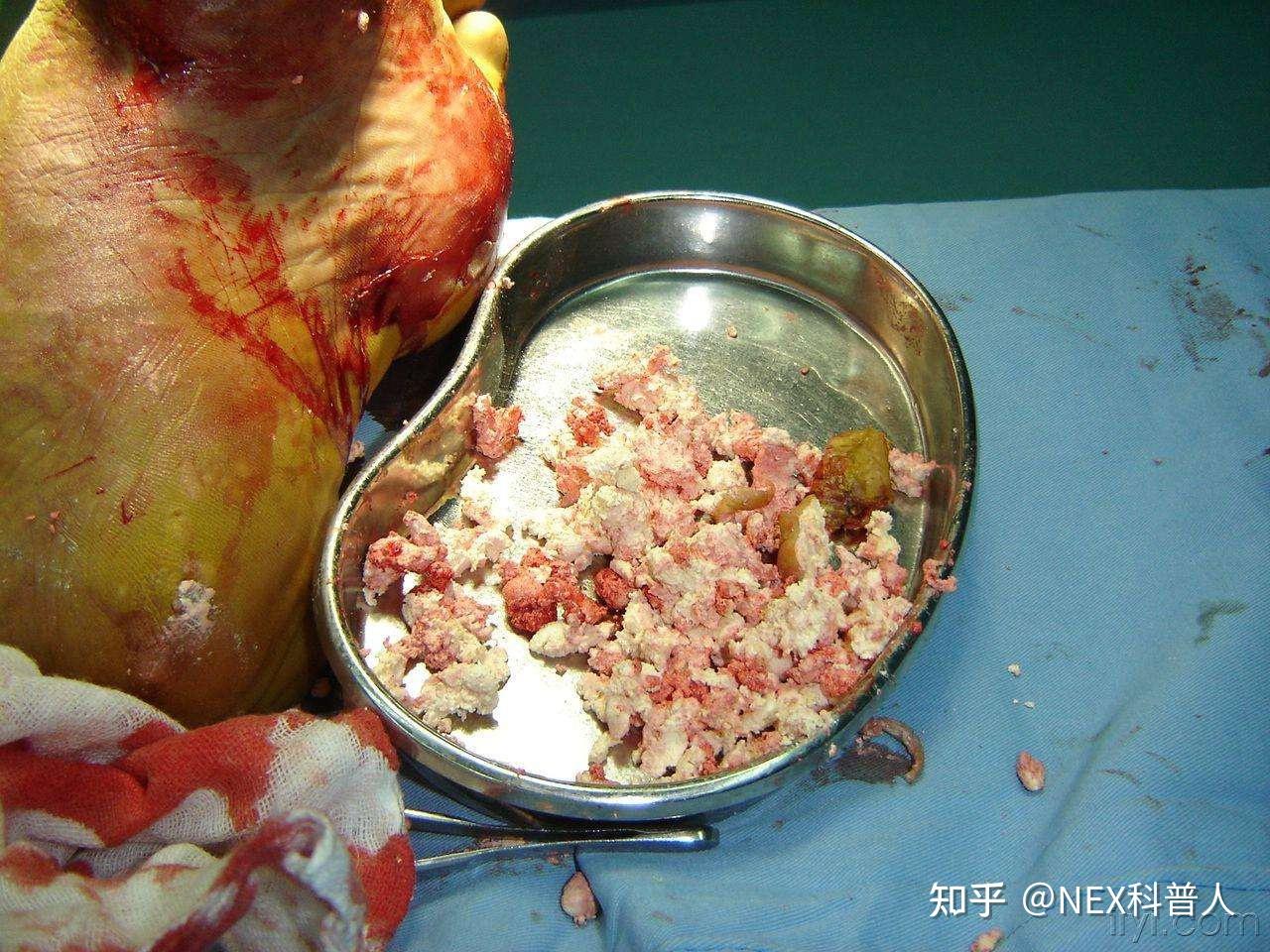
二、痛风石偏好于在肢体末端关节处形成的原因
临床上,痛风石常见于足背、踝、足跟、膝、腕、指、肘、耳廓等多个肢体末端关节
原因有以下 3 点:
1. 关节腔与血液之间难以实现物质交换:
关节腔与血液之间的物质交换,除了需要跨过血管壁外,还要跨过滑囊膜及软骨
致使关节内的尿酸与血尿酸之间难以实现交换,即便进行降尿酸治疗,血尿酸显著降低,关节内的尿酸也很难被快速转运至血液中,因此尿酸盐易在此部位结晶沉积。
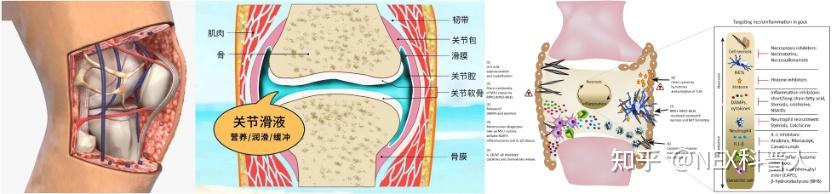
左图为关节血管、中图为关节结构示意图、右图为痛风石
2. 肢体末端温度低
人体温度场分布是不均匀的,不同部位的温度有所不同。
一般来说,人体的核心部位温度较高,而四肢和头部温度较低。
人体的核心部位包括头部、胸部和腹部,这些部位的温度通觉在 36.5°C~37.5°之间。
而四肢的温度通常在 32°C到 35°C之间。这是因为四肢的血管较为丰富,血液循环较快,散热较快,所以温度较低。
另外,关节处由于脂肪含量比较低,相较于其他部位,肢体末端的体表温度与深部温度差更大
在环境温度为 23℃时测定,额部的皮肤温为33~34℃,躯干为32℃,手为30℃,足为27℃。在寒冷的环境中,随着气温下降,四肢末梢(手和足)的皮肤温度显著降 低,而头部皮肤温的变动相对比较少
尿酸盐溶解度跟温度息息相关,在37℃的生理盐水中,尿酸盐溶解度可达到416 μmol/L。当体温是25℃时,尿酸盐溶解度会大幅度下降。
然而肢体末端,尤其是大脚趾的温度约25℃,难以溶解尿酸钠,使得尿酸盐结晶体在第一跖趾关节沉积。
3. 关节频繁活动且易受到损伤
肢体末端的关节损伤后
软骨蛋白多糖、硫酸软骨素、人血清白蛋白浓度会降低,导致尿酸盐溶解度降低,促进尿酸盐晶体形成[13]。
抗体蛋白会升高,尿酸盐晶体会粘附抗体蛋白,增强促炎活性,促进尿酸盐晶体成核、增长[13]。
尤其第一跖趾关节是小关节,在肢体末端,承受的压力较大,易受到损伤。
关节受到损伤后,会使得细小尿酸盐结晶脱落,进而诱发痛风。
痛风每发作一次,痛风石就会长大一分!!!
三、很多人在处于无症状高尿酸血症阶段时,就出现了痛风石
随着新的更敏感、更特异的影像学检查方法的广泛应用,无症状高尿酸血症与痛风的界限渐趋模糊。
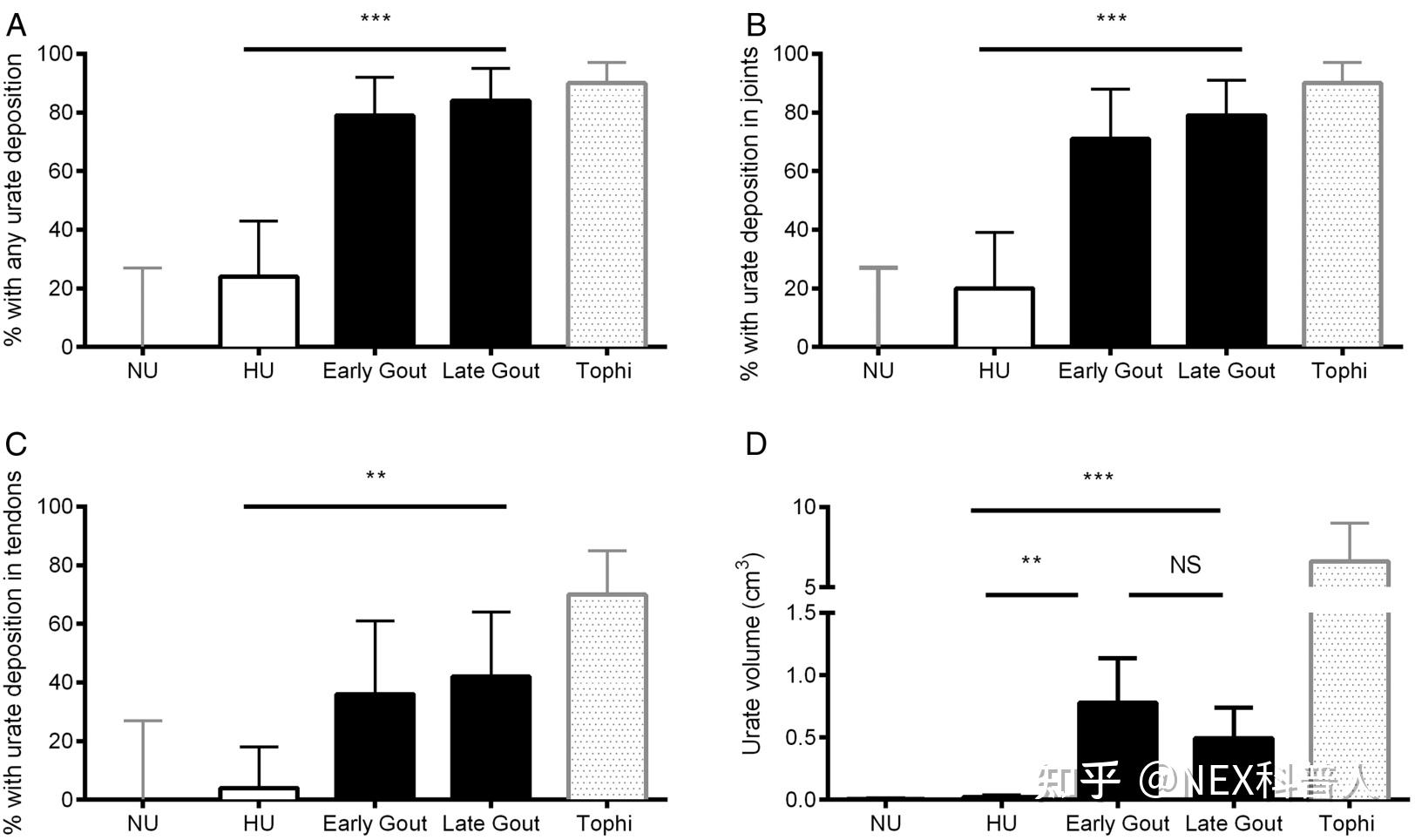
Dalbeth N 等研究人员用双能 CT 检测了血清尿酸值≥540 μ mol/L的无症状高尿酸血症患者(共 25 人)和痛风患者(共 33 人)的足部,发现[16]:
6/25 (24%) 的无症状高尿酸血症患者、11/14 (79%) 的早期痛风患者(疾病持续时间≤3 年)和 16/19 (84%) 的晚期痛风患者中发现了尿酸盐晶体的沉积(p<0.001)。
无症状高尿酸血症组在关节和肌腱均观察到尿酸盐晶体,但明显少于于痛风组(p≤0.001的关节和肌腱部位)。
与痛风早期和晚期组相比,无症状高尿酸血症组的尿酸沉积体积也显著降低(p<0.01)。
早期和晚期痛风组沉积的尿酸盐晶体总体积相近且无明显差异。
因此,高尿酸血症与痛风是一个连续、慢性的病理生理过程,其临床表型具有显著的异质性。部分无症状高尿酸血症患者关节内也存在尿酸盐晶体,甚至出现周围组织的损伤,如骨侵蚀。
这一结果也被 Wang P 等研究人员证实:在 130 名年龄 ≥40 岁的代谢综合征患者中,筛查血清尿酸(sUA)水平≥390 μmol/L,其中 46 人进行了足部/踝关节DECT扫描[17]。
46 例患者中有 7 例(15%)通过双能 CT 检测到尿酸盐晶体沉积积,平均体积为 0.13±0.14 cm3。在单变量分析中,血尿酸水平与尿酸盐晶体沉积的总体积呈适度的线性关系(β=0.11, P=0.09)。

参考文献:
1. Schett G, Schauer C, Hoffmann M, Herrmann M. Why does the gout attack stop? A roadmap for the immune pathogenesis of gout. RMD Open. 2015 Aug 15;1(Suppl 1):e000046. doi: 10.1136/rmdopen-2015-000046. PMID: 26557370; PMCID: PMC4632150.
2. Chhana A, et al. BMC Musculoskelet Disord. 2015 Oct 14;16:296. doi: 10.1186/s12891-015-0762-4. PMID: 26467213; PMCID: PMC4606994.
3. Ahmad MI, Masood S, Furlanetto DM, Nicolaou S. Urate Crystals; Beyond Joints. Front Med (Lausanne). 2021 Jun 4;8:649505. doi: 10.3389/fmed.2021.649505.
4. Choi HK, Al-Arfaj AM, Eftekhari A, Munk PL, Shojania K, Reid G, Nicolaou S. Dual energy computed tomography in tophaceous gout. Ann Rheum Dis. 2009 Oct;68(10):1609-12. doi: 10.1136/ard.2008.099713.
5. Christiansen SN, Müller FC, Østergaard M, Slot O, Møller JM, Børgesen HF, Gosvig KK, Terslev L. Dual-energy CT in gout patients: Do all colour-coded lesions actually represent monosodium urate crystals? Arthritis Res Ther. 2020 Sep 11;22(1):212. doi: 10.1186/s13075-020-02283-z.
6. Mallinson PI, Reagan AC, Coupal T, Munk PL, Ouellette H, Nicolaou S. The distribution of urate deposition within the extremities in gout: a review of 148 dual-energy CT cases. Skeletal Radiol. 2014 Mar;43(3):277-81. doi: 10.1007/s00256-013-1771-8.
7. Toprover M, Krasnokutsky S, Pillinger MH. Gout in the Spine: Imaging, Diagnosis, and Outcomes. Curr Rheumatol Rep. 2015 Dec;17(12):70. doi: 10.1007/s11926-015-0547-7.
8. Klauser AS, Halpern EJ, Strobl S, Gruber J, Feuchtner G, Bellmann-Weiler R, Weiss G, Stofferin H, Jaschke W. Dual-Energy Computed Tomography Detection of Cardiovascular Monosodium Urate Deposits in Patients With Gout. JAMA Cardiol. 2019 Oct 1;4(10):1019-1028. doi: 10.1001/jamacardio.2019.3201.
9. Klauser AS, Strobl S, Schwabl C, Klotz W, Feuchtner G, Moriggl B, Held J, Taljanovic M, Weaver JS, Reijnierse M, Gizewski ER, Stofferin H. Prevalence of Monosodium Urate (MSU) Deposits in Cadavers Detected by Dual-Energy Computed Tomography (DECT). Diagnostics (Basel). 2022 May 16;12(5):1240. doi: 10.3390/diagnostics12051240.
10. Euler A, Wullschleger S, Sartoretti T, Müller D, Keller EX, Lavrek D, Donati O. Dual-energy CT kidney stone characterization-can diagnostic accuracy be achieved at low radiation dose? Eur Radiol. 2023 Mar 29. doi: 10.1007/s00330-023-09569-1.
11. Gutjahr R, Polster C, Henning A, Kappler S, Leng S, McCollough CH, Sedlmair MU, Schmidt B, Krauss B, Flohr TG. Dual Energy CT Kidney Stone Differentiation in Photon Counting Computed Tomography. Proc SPIE Int Soc Opt Eng. 2017 Mar;10132:1013237. doi: 10.1117/12.2252021.
12. Pund EE, Hawley RL, McGee HJ, Blount SG. Gouty heart. N Eng J Med. (1960) 263:835–8. doi: 10.1056/NEJM196010272631705
13. Chhana A, Lee G, Dalbeth N. Factors influencing the crystallization of monosodium urate: a systematic literature review. BMC Musculoskelet Disord. 2015 Oct 14;16:296. doi: 10.1186/s12891-015-0762-4.
14. Iwata H, Nishio S, Yokoyama M, Matsumoto A, Takeuchi M. Solubility of uric acid and supersaturation of monosodium urate: why is uric acid so highly soluble in urine? J Urol. 1989 Oct;142(4):1095-8. doi: 10.1016/s0022-5347(17)39003-1. PMID: 2795738.
15. Schorn C, Janko C, Munoz L, Schulze C, Strysio M, Schett G, Herrmann M. Sodium and potassium urate crystals differ in their inflammatory potential. Autoimmunity. 2009 May;42(4):314-6. doi: 10.1080/08916930902832058. PMID: 19811287.
16. Dalbeth N, House ME, Aati O, Tan P, Franklin C, Horne A, Gamble GD, Stamp LK, Doyle AJ, McQueen FM. Urate crystal deposition in asymptomatic hyperuricaemia and symptomatic gout: a dual energy CT study. Ann Rheum Dis. 2015 May;74(5):908-11. doi: 10.1136/annrheumdis-2014-206397.
17. Wang P, Smith SE, Garg R, Lu F, Wohlfahrt A, Campos A, Vanni K, Yu Z, Solomon DH, Kim SC. Identification of monosodium urate crystal deposits in patients with asymptomatic hyperuricemia using dual-energy CT. RMD Open. 2018 Mar 9;4(1):e000593. doi: 10.1136/rmdopen-2017-000593. |